熱力學定律是什麼?概念、特點和例子、起源和演變歷史
我們解釋了熱力學定律是什麼,它們是什麼,以及它們的特點和例子。此外,它的起源和演變的歷史。

熱力學定律是什麼?
熱力學定律(或熱力學原理)描述了三個基本物理量溫度這能源和熵,這是熱力學系統的特徵。它們對於理解宇宙以及某些現象的不可能性,例如運動永久。
熱力學有四個定律:
-
熱力學零定律
-
熱力學第一定律
-
熱力學第二定律
-
熱力學第三定律
在數學上,這些原理由一組方程來描述,這些方程解釋了熱力學系統的行為,熱力學系統被定義為任何研究物件(從分子或人,添加到大氣層或在平底鍋中燒開水)。
“熱力學”一詞來自希臘語 thermos,意思是”熱“和 dynamos,意思是”強度”.
您可能對以下內容感興趣:熱力學
熱力學“零”定律
“零定律”在邏輯上表示如下:如果 A = C 且 B = C,則 A = B。
“零定律”以這個名字為人所知,儘管它是最後一個運行的。該原理也稱為熱平衡定律,它規定:「如果兩個系統與第三個系統獨立處於熱平衡狀態,則它們也必須彼此處於熱平衡狀態。它可以邏輯地表示如下:如果 A = C 且 B = C,則 A = B。
該定律允許我們比較熱能三個不同的身體 A、B 和 C。如果物體 A 與物體 C 處於熱平衡狀態(它們具有相同的溫度),並且 B 也與 C 具有相同的溫度,則 A 和 B 具有相同的溫度。
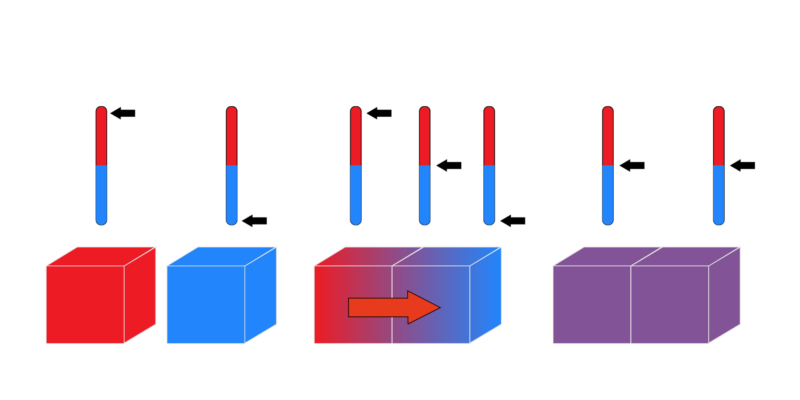
陳述這一原理的另一種方式是論證當兩個溫度不同的物體接觸時,它們會交換熱量,直到它們的溫度相等。
這項法律的日常例子很容易找到。當我們進入熱水或冷水中時,我們只會在最初的幾分鐘內注意到溫差,因為然後我們的身體會進入熱平衡水我們將不再注意到差異。當我們進入熱室或冷室時,也會發生同樣的情況:我們一開始會注意到溫度,但隨後我們將停止感知差異,因為我們將與它進入熱平衡。
另請參閱:熱平衡
熱力學第一定律

能量不能被創造或摧毀,只能被轉化。
第一部法律被稱為「節能法」,因為它規定在任何系統與環境物理隔離,能量總量始終相同,即使它可以從一種形式的能量轉化為不同的能量。或者換句話說:能量不能被創造或摧毀,只能被轉化。
因此,當向物理系統提供給定的熱量 (Q) 時,其總能量可以計算為提供的熱量減去工作(W) 受系統對其周圍環境的影響。用公式表示:ΔU = Q – W。
作為該定律的一個例子,讓我們想像一架飛機的發動機。它是一個熱力學系統,由燃料組成,燃料在燃燒、釋放熱量並執行功(使飛機移動)。所以:如果我們能測量完成的功和釋放的熱量,我們就可以計算出系統的總能量,並得出結論,發動機中的能量在飛行過程中保持不變:能量既沒有被創造也沒有被破壞,而是被要求改變它的化學能自熱能和動能(運動,即工作)。
另請參閱:能量守恆原理
熱力學第二定律
如果有足夠的時間,所有系統最終都會趨於不平衡。
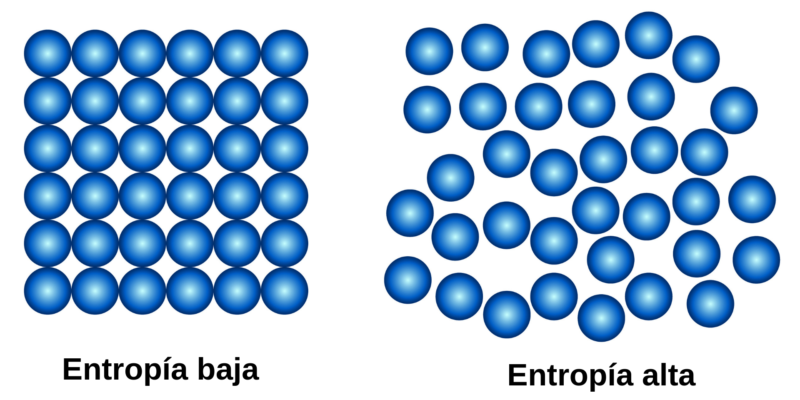
第二定律,也稱為「熵定律」,可以概括如下:宇宙中的熵量在時間.這意味著系統的無序程度會增加,直到達到平衡點,這是系統最無序的狀態。
該定律引入了物理學中的一個基本概念:熵的概念(由字母 S 表示),在物理系統的情況下,它代表無序的程度。事實證明,在每一個能量轉化的物理過程中,一定量的能量是不可用的,也就是說,它不能做功。如果你不能做工作,在大多數情況下,這種能量就是熱量。系統釋放的熱量,它的作用是增加系統的無序性,即它的熵。熵是系統無序程度的度量。
該定律的公式指出,熵的變化 (dS) 將始終等於或大於傳熱 (dQ) 除以系統的溫度 (T)。換句話說:dS ≥ dQ / T。
要通過一個例子來理解這一點,燃燒一定量的事然後收集產生的灰燼。當我們稱量它們時,我們會發現它的物質比它的初始狀態要小:物質的一部分以氣體他們無法在系統上執行工作,這導致了系統的無序。
另請參閱:傳熱
熱力學第三定律

當您達到絕對零度時,物理系統的過程就會停止。
第三定律指出,達到絕對零度的系統的熵將是一個確定的常數。換句話說:
-
當達到絕對零度(以開爾文單位為單位為零)時,物理系統的過程停止。
-
當它達到絕對零(以開爾文單位表示為零)時,熵具有恆定的最小值。
每天很難達到所謂的絕對零度 (-273.15 °C),但我們可以通過分析冰箱中發生的情況來思考這一定律:食品我們存放在那裡會冷卻很多,以至於它們內部的生化過程會減慢甚至停止。這就是為什麼它的分解是遲緩的,而它的消費持續時間更長。
另請參閱:熵
熱力學定律的歷史
熱力學的四個原理有不同的起源,有些是從以前的原理中制定出來的。事實上,第一個建立的是第二個,即法國物理學家和工程師尼古拉斯·萊昂納德·薩迪·卡諾 (Nicolas Léonard Sadi Carnot) 於 1824 年的工作。
然而,在 1860 年,魯道夫·克勞修斯 (Rudolf Clausius) 和威廉·湯普森 (William Thompson) 重新制定了這一原理,增加了我們現在所說的熱力學第一定律。後來,第三個出現了,也被稱為“Nerst 的假設”,因為它的出現要歸功於 Walther Nernst 在 1906 年至 1912 年間的研究。
最後,所謂的「零定律」出現在 1930 年,由古根海姆和福勒提出。應該說,它並不是在所有領域都被認為是真正的法律。